Teorie
Atomové jádro
Atomová jádra v přírodě se běžně vyskytující hmoty se skládají z protonů a neutronů. Mají tedy kladný náboj a je v nich soustředěna téměř veškerá hmotnost atomů (elektrony mají oproti protonům a neutronům zhruba 2000-krát menší hmotnost). Počet protonů v jádře označujeme protonovým číslem Z (souvisí s nábojem jádra), počet neutronů číslem neutronovým N a celkový počet nukleonů (protonů a neutronů) udává číslo nukleonová A (A = Z + N, souvisí s hmotností jádra). Na základě počtu protonů a neutronů v jádře zavádíme pojmy nuklid, izotop a izobar.
Nuklid – představuje soubor stejných atomů, jejichž jádra tedy mají stejná složení. To vyjadřujeme zápisem , kde X představuje chemickou značku, např. . Jelikož počet protonů v jádře je dán chemickou značkou, píšeme častěji zkráceně , takže například zápis udává Z = 90 (pořadí thoria v periodické tabulce prvků) a N = 232 – 90 = 142.
Izotopy – jsou nuklidy, které mají stejné protonové, ale různé nukleonové (a tedy i neutronové) číslo. Takže například řekneme, že , a jsou různé izotopy uhlíku.
Izobary – jsou nuklidy, které mají stejné nukleonové, ale různé protonové číslo, např. , a .
Protony a neutrony sídlí v atomovém jádře ve velmi malém objemu, takže protony jsou navzájem velmi silně odpuzovány elektrostatickou (Coulombovou) silou. Stabilitu jádra zajišťuje jaderná síla, která má velmi krátký dosah (10–15 m) a je mnohem silnější než síla elektrostatická. Podstata této síly spočívá ve výměně virtuálních částic tzv. gluonů.
Radioaktivita
Z více než 2000 známých nuklidů je jen 266 stálých. Ostatní, ať se nacházejí v přírodě nebo vznikají jadernými reakcemi, se více nebo méně rychle samovolně přeměňují na jiné nuklidy – jsou radioaktivní.
Radioaktivitou tedy rozumíme schopnost některých atomových jader vysílat záření. Přitom se takové jádro může změnit v jiné nebo alespoň ztratí část své energie. Při jaderné přeměně se proměňuje struktura jádra, izotop jednoho prvku se mění v izotop prvku jiného. Empiricky bylo zjištěno, že jádra jsou stálá, tj. nepodléhají radioaktivním přeměnám, pouze při určitém poměru N/Z. U stabilních lehkých jader (Z ≤ 20) je tento poměr roven jedné (výjimkou jsou jádra a ), u hmotnějších jader se dále zvětšuje až po hodnotu 1,52 u nejtěžšího stabilního nuklidu . Pokud složení jádra vybočí z optimálního poměru mezi protony a neutrony, stává se radioaktivním. Některé prvky mají jen jeden stabilní izotop, zatímco u jiných existují stabilní izotopy dva i více.
Rozeznáváme tři skupiny radioaktivních přeměn:
přeměny, při nichž se mění Z při konstantním A (přeměny β– a β+, elektronový záchyt)
přeměny, při nichž se současně mění Z i A (přeměna α, emise nukleonů, emise těžších jader, samovolné štěpení)
přeměny způsobené deexcitací jádra, při nichž se mění pouze energetický obsah jádra (emise záření γ, vnitřní konverze).
Mechanizmus ztráty energie ionizujícího záření
Záření emitované radioaktivními nuklidy představuje proud hmotných částic a fotonů. Jejich energie leží v řádech keV až MeV, což jsou hodnoty o několik řádů převyšující ionizační energii atomů a molekul. Z tohoto důvodu při průchodu látkou způsobuje intenzivní ionizaci (odtud pak i název ionizující záření). Kromě ionizace dochází i k excitaci atomů a molekul. Elektrony uvolněné při ionizaci mají takovou energii, že samy způsobují sekundární ionizaci a excitaci.
Každou jednotlivou ionizací či excitací se zmenšuje energie ionizující částice o příslušnou hodnotu ionizační či excitační energie. Vzhledem k tomu, že tato energie představuje jen malou část energie částice, vzniká podél dráhy ionizující částice velké množství iontů, volných elektronů a excitovaných stavů. Tím částice odevzdává látce svou energii, až postupně ztratí schopnost ionizace a excitace a je v prostředí absorbována. Je-li vrstva látky dostatečně silná, všechny částice předají látce veškerou svou energii a záření je zcela absorbováno. Tloušťka vrstvy, která úplně absorbuje záření, se označuje jako dosah záření.
V našem experimentu budeme zkoumat absorpci záření β (zářič 90Sr), dále se tedy zabýváme jen jeho absorpčním mechanismem.
Mechanismus absorpce β záření: 1)
Lineární přenos energie β záření je obecně menší, než je tomu kupříkladu u záření α. Příčinou je menší velikost náboje elektronu oproti velikosti náboje jádra hélia a fakt, že při dané energii je rychlost elektronů výrazně vyšší. Z tohoto důvodu má β záření v prostředí větší pronikavost a dosah.
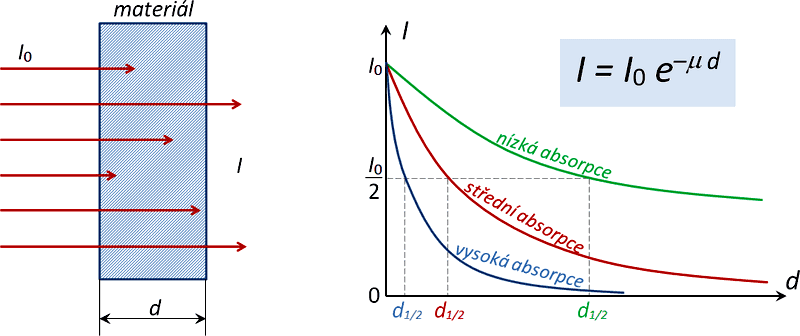
Obr. 1 – Základní zákonitosti absorbce ionizujícího záření v látce hustoty ρ, protonového čísla Z a tloušťky d.
V plynech (podle energie záření) je dosah několik metrů, β záření o nízké energii se malým dosahem podobá α záření. Absorpční křivka β záření má exponenciální průběh, který pro intenzitu záření popisuje empirický vztah: 2)
kde I0 je počáteční intenzita záření, d je tloušťka absorbující vrstvy a μ je lineární absorpční koeficient (nebo též lineární součinitel zeslabení). Ten je závislý na hustotě elektronů prostředí a energii záření. Jeho hodnota závisí na hustotě a protonovém čísle absorpčního materiálu a výrazně též na energii záření. Můžeme pro něj psát:
kde ρ je hustota prostředí a konstanta μm, která je již nezávislá na hustotě, se nazývá hmotnostní absorpční koeficient (též hmotnostní zeslabovací koeficient) pro daný typ záření a příslušné energetické spektrum. Dále, zvláště pro technické účely – jako je kupříkladu návrh stínění, se místo lineárního součinitele zeslabení v tabulkách uvádí hodnota tzv. polovrstvy (polotloušťky) absorpce , což je taková tloušťka vrstvy daného materiálu, která zeslabí intenzitu daného záření na polovinu.
- 1)
- K absorpci β záření v menší míře přispívá i vznik brzdného (RTG) a tzv. Čerenkovova záření.
- 2)
- Základní vlastností exponenciální funkce se záporným exponentem je, že se blíží nule až v limitě v nekonečnu. To by znamenalo, že záření prakticky nikdy nelze úplně odstínit. Tak je tomu však jen teoreticky. Ve skutečnosti každý zářič emituje jen konečný počet částic. Po průchodu dostatečnou tloušťkou (desítky či stovky d1/2) se v praxi vždy nakonec pohltí i poslední částice.






